
Científicos de la UNAB modifican actividad de un gen y mejoran funciones cognitivas en modelos de Alzheimer y envejecimiento
El estudio –liderado por los académicos de la UNAB Brigitte van Zundert y Martin Montecino – implicó la modificación epigenética de un gen e involucró el trabajo en colaboración con científicos en Chile, EEUU y Holanda. El trabajo fue publicado en la revista Brain.
La demencia consiste en un conjunto de síntomas asociados a la pérdida gradual y progresiva de funciones cognitivas. Si bien la mayor parte del tiempo los primeros síntomas aparecen en la tercera edad, es posible que también sea diagnosticada en personas jóvenes. Actualmente en el mundo hay casi 50 millones de personas diagnosticadas con Alzheimer –el tipo de demencia más común– y se proyecta que este número llegará a más de 131 millones para el año 2050 (World Alzheimer Report, 2016). La enfermedad de Alzheimer da cuenta de entre el 50 y 70% de todos los casos de demencia que se diagnostican en el mundo y no tiene cura. En Chile, se estima que unas 180 mil personas viven con Alzheimer y –considerando que cerca de un tercio de las personas mayores de 85 años padece de esta enfermedad y que la esperanza de vida ha ido aumentando de manera progresiva– se estima que se convertirá en un serio problema de salud pública.
Genética y epigenética
Actualmente se sabe que el desarrollo de la enfermedad de Alzheimer está asociado tanto a factores genéticos como ambientales. Entre los genes que han despertado el interés de los científicos por su posible vinculación al desarrollo de enfermedades neurodegenerativas está PSD95. Este gen proporciona las instrucciones para que el cuerpo fabrique una proteína llamada PSD-95, y se ha demostrado que esta proteína es muy importante para el correcto funcionamiento de las neuronas, participando en procesos asociados a plasticidad neuronal (cambios en el cerebro a escala de neurona o de cerebro completo) y estabilización de circuitos neuronales.
En modelos murinos (como ratones o ratas) de la enfermedad de Alzheimer se había reportado una disminución en la actividad del gen PSD95 y de la abundancia de su producto (la proteína PSD-95), por lo que se sospechaba que podría ser un blanco interesante para una aproximación terapéutica ¿Sería posible que la modificación de la actividad de este gen mejore las funciones cognitivas en modelos murinos de la enfermedad de Alzheimer? Entre las aproximaciones experimentales para controlar la actividad de este gen están las herramientas de la epigenética, que permiten modificar la actividad de un gen sin alterar su secuencia (modificando por ejemplo a las proteínas que activan o reprimen la función de un gen). De esta forma, la posibilidad de modificar de manera experimental la actividad del gen PSD95 usando herramientas epigenéticas se proyectaba como una posibilidad muy interesante
Hackeando el genoma
Para confirmar si era posible modificar la actividad del gen PSD95, científicos de la Universidad Andrés Bello –liderados por Brigitte van Zundert y Martin Montecino, académicos del Centro de Investigaciones Biomédicas (CIB) de la Facultad de Ciencias Biológicas y Facultad de Medicina– trabajando en colaboración con científicos del Centro Médico de la Universidad de Groningen (Holanda), de la Universidad de Massachusetts (EEUU), y de las Universidades de Chile, Católica de Chile, de Valparaíso y de Los Andes (Chile) generaron una herramienta molecular, llamada factor de transcripción artificial, que se une específicamente al gen PSD95 y que causa, a través de cambios en su perfil epigenético, un aumento en su expresión. Esta técnica, que se denomina edición del epigenoma, permite normalizar la expresión de PSD95.
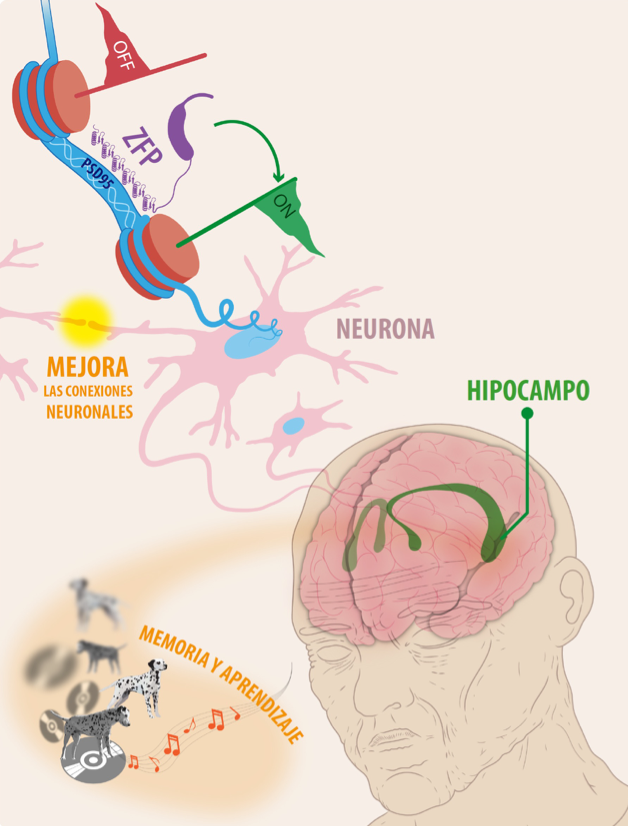
A nivel microscópico, la alteración de la función del gen PSD95 tuvo varios impactos, particularmente a nivel de la plasticidad neuronal en una zona del cerebro llamada hipocampo, que es muy relevante en funciones tanto motoras como cognitivas. Sin embargo, los resultados más sorprendentes se relacionan con algunos ensayos cognitivos realizados con los modelos del estudio. En efecto, tanto en animales viejos como en aquellos usados como modelo para la enfermedad de Alzheimer, se evidenció un mejor desempeño en test cognitivos y de memoria cuando expresaban el factor de transcripción artificial que activa al gen PSD95.
De esta forma, este estudio establece que la edición del epi-genoma podría convertirse en una potencial terapia para pacientes humanos que manifiesten algún tipo de desorden neurológico asociado a la función de la proteína PSD-95, como la enfermedad de Alzheimer. Si bien hoy existen diferentes técnicas para editar el genoma (es decir, cambiar la información genética) la edición del epigenoma podría resultar en una mejor alternativa terapéutica. “Técnicas como CRISPR/Cas-9 permiten editar el genoma; sin embrago, su baja eficiencia y los muchos blancos inespecíficos generados, hacen que aún se requiera de mucho desarrollo de la tecnología como para poder ser utilizada de manera segura”, señala la Dra. van Zundert.
¿Y en humanos?
Sobre el potencial terapéutico de esta aproximación, la Dra. van Zundert señala que “la limitante en este momento es el transporte de la herramienta molecular a las zonas afectadas en el cerebro humano, como el hipocampo. Para esto se requieren vectores virales que son virus modificados (que no causan enfermedades) y que funcionen como vehículo para introducir material genético exógeno (como nuestra herramienta molecular) en el núcleo de las células. Hay múltiples estudios clínicos en EEUU que usan vectores virales para determinar su seguridad y su capacidad de entregar herramientas moleculares para terapia génica. Los avances han sido notorios, especialmente para regiones periféricas del cuerpo (por ejemplo, músculo) donde la entrega de los vectores virales se hace mediante inyecciones locales. Llegar al cerebro es mucho más complicado y por esta razón los estudios clínicos han sido más lentos.”
Es la primera vez que se utiliza una terapia epi-genética de esta naturaleza en Alzheimer, por lo que las proyección de este estudio son muy interesantes y se podrían aplicar junto con otras aproximaciones terapéuticas para mejorar la vida de los pacientes con Alzheimer.
Otro aspecto destacable del estudio es su carácter colaborativo. “Este trabajo, comenzó hace 7 años, y sólo fue posible concretarlo gracias al apoyo financiero de CONICYT y el trabajo unos 22 colaboradores, entre estudiantes, postdoctorados e investigadores de la UNAB (Dra. Lorena Varela), U. de Massachusetts (Dr. Miguel Esteves), U. Chile (Dr. Steffen Hartel), U. Valparaíso (Dr. Marco Fuenzalida), U. de los Andes (Dra. Ursula Wyneken) y PUC-CARE (Dr. Nibaldo Inestrosa). Sin estos colaboradores, simplemente no se puede lograr estos tipos de descubrimientos que, esperamos, tendrán un impacto importante para pacientes con demencia en Chile y el mundo.
La Dra. van Zundert espera ahora poder seguir trabajando en colaboración y sumar a este esfuerzo a alguna compañía que se muestre interesada por estos hallazgos, para así iniciar un ensayo clínico con voluntarios que padezcan demencia.
Estudio:
Epigenetic editing of the Dlg4/PSD95 gene improves cognition in aged and Alzheimer’s disease mice. Bustos FJ, Ampuero E, Jury N, Aguilar R, Falahi F, Toledo J, Ahumada J, Lata J, Cubillos P, Henríquez B, Guerra MV, Stehberg J, Neve RL, Inestrosa NC, Wyneken U, Fuenzalida M, Härtel S, Sena-Esteves M, Varela-Nallar L, Rots MG*, Montecino M*, van Zundert B*. Brain (2017) Accepted. DOI 10.1093/brain/awx272
https://doi.org/10.1093/brain/awx272 (link disponible desde 16 Noviembre 2017 en “advanced article”)
